药品GMP现场检查缺陷项目整改要求食药监药化监
附件5
药品GMP现场检查缺陷项目整改要求
为实践科学监管理念,规范企业缺陷整改报告撰写,引导企业采取有效措施对现场检查发现的缺陷进行整改,提升药品生产企业生产质量管理水平,根据《药品生产质量管理规范(2010年修订)(卫生部令第79号)》和《药品生产质量管理规范认证管理办法》(国食药监安[2011]365号),制订本指导原则。
一、总则
1、本指导原则适用于药品GMP认证、跟踪检查等缺陷项目的整改;
2、企业整改时应按照药品GMP理念,深入分析缺陷产生原因,对现场检查所发现的缺陷进行风险评估,区分缺陷是否属于系统性缺陷,举一反三,措施得当,确保整改到位;
-1 -
3、企业自检发现缺陷项目的整改也可参照此原则实施。
二、缺陷整改程序
现场检查结束后,原则上企业应在20个工作日内向省级药品检查机构报送缺陷整改报告,如无法在规定时限内完成整改,企业可报送相应的整改计划。
三、整改报告要求
1、整改报告的基本要求
(1)整改报告由正文和附件两部分组成。
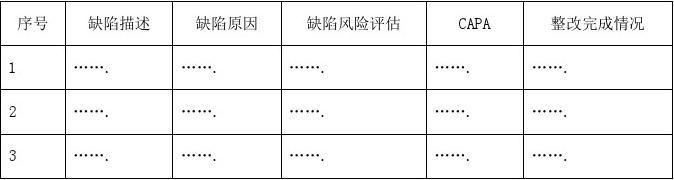
正文部分至少应包括:缺陷的描述、缺陷原因的分析、缺陷的风险评估、纠正及预防措施、采取措施后的有效性评价、整改完成情况。正文部分表述可以是文字,也可以采用以下表格形式(表1)。
表1 整改正文表
-2 -
附件部分应是与正文中每个缺陷相对应的证明性材料。
(2)整改报告应针对缺陷项目,内容真实完整,数据清晰,表达清楚,文字通顺,用语准确,如实反映企业的整改落实情况,并加盖企业公章(每页或骑缝章)。
2、整改报告的具体要求
(1)整改报告正文的具体要求
缺陷描述。企业可提供不合格项目情况表复印件,并针对相应的缺陷进行详细的描述,如发生的时间、地点、数据、具体情节及相关人员等,文字表达应准确无误。
缺陷原因分析。企业应对缺陷产生的原因进行分析,分析要深入查找缺陷发生的根本原因:
1)如涉及软件的,企业应分析是否制订了相应的文件;相应的文件内容是否完善、合理;相关文件是否进行了培训;员工是否按照文件要求操作;质量管理部门是否进行了有效的监督控制。
-3 -
2)涉及硬件的,主要从设计选型、施工安装、日常维护、验证等进行原因分析,并审阅支持该硬件的文件系统。整改资料中应附改造后的设施设备图片、影音资料等。
3)涉及人员的,是否配备了足够的人员、相关人员是否胜任该岗位的需要、相关人员是否接受了应有的培训、培训的内容是否已被熟练掌握。
缺陷的风险评估。企业应对涉及的缺陷逐条进行风险评估,风险评估可采用FMEA(失效模式与影响分析)方法,也可采用其他评估方法。
FMEA法风险评估要素如下:
1)该缺陷产生的直接后果,对产品质量是否产生直接的不良影响或潜在的影响。即严重性(S);
2)该缺陷可能发生的频率的高低。即重现性(O);
3)该缺陷是否易被观察或检测到。即可检测性(D);
4)通过以上三个指标判断该缺陷的风险系数RPN;
-4 -
5)企业应评估该缺陷涉及的范围,是否涉及本次检查范围外的产品;
6)形成最终的评估结果,依据风险系数评定缺陷风险等级。
纠正及预防措施。具体应包含以下内容:
1)企业根据风险评估的结果,针对缺陷产生原因,在企业内部进行全面排查,举一反三,分析关联性环节是否存在同样问题,如相邻批次、其他车间相同工序等,提出采取或拟采取的纠正措施;对有可能再次发生的缺陷提出明确的预防性措施,以防止此类缺陷的再次发生;
2)采取的整改措施和预防措施应明确相关的责任部门和责任人,并明确完成时间;
3) 如评估认为缺陷对已经生产或上市的产品产生质量风险的,企业应明确是否需要采取进一步的产品控制措施,包括停止生产、拒绝放行、停止销售、召回、销毁等。具体应提供
-5 -
产品的名称、规格、批次、数量、销售流向等内容。
整改完成情况。企业应明确整改是否已全部完成,完成责任部门,人员及完成的时间。如采取的纠正预防措施短期内不能完成,可上报整改计划,明确整改方案及完成时间。
采取措施后的有效性评价。企业应简要描述采取的措施是否可有效杜绝缺陷再次发生。
(2)整改报告附件的具体要求
附件中应提供已(拟)采取的纠正措施或预防措施的证明性材料:
1)涉及关键岗位人员调整的,应提供相应的任免文件、相关人员的资质证明、人员工作经历复印件;
